La galvanoplastia o electrodeposición es una aplicación práctica de la electroquímica. Se trata de una técnica basada en los principios eléctricos y químicos, en donde se aplica una o varias capas de un metal seleccionado sobre un objeto receptor, por lo general, también metálico. La galvanoplastia o electrodeposición permite aplicar a un objeto metálico una capa fina, no mayor a 20 μm, para dar características anticorrosivas o simplemente para hacer más resistente el objeto.
Para ello, se requiere de un medio electrolítico que contenga iones del metal que se colocará sobre el objeto. Generalmente, se disuelven sales ricas en el metal deseado en agua y se hace pasar una corriente eléctrica controlada para lograr la ejecución de la electrodeposición.
El nombre de galvanoplastia se debe a Luigi Galvani (Bolonia, Italia, 1737-1798) quien fue un médico, fisiólogo y físico italiano. Sus estudios le permitieron descifrar la naturaleza eléctrica del proceso que lleva su nombre, fundando la ingeniería electroquímica que estudia las baterías eléctricas, además de descubrir el impulso nervioso, determinando los principios de la biofísica. Galvani y Alessandro Volta fueron colegas en la Universidad de Pavía y trabajaron en conjunto en el incipiente tema de la electroquímica.
Para ello, se requiere de un medio electrolítico que contenga iones del metal que se colocará sobre el objeto. Generalmente, se disuelven sales ricas en el metal deseado en agua y se hace pasar una corriente eléctrica controlada para lograr la ejecución de la electrodeposición.
El nombre de galvanoplastia se debe a Luigi Galvani (Bolonia, Italia, 1737-1798) quien fue un médico, fisiólogo y físico italiano. Sus estudios le permitieron descifrar la naturaleza eléctrica del proceso que lleva su nombre, fundando la ingeniería electroquímica que estudia las baterías eléctricas, además de descubrir el impulso nervioso, determinando los principios de la biofísica. Galvani y Alessandro Volta fueron colegas en la Universidad de Pavía y trabajaron en conjunto en el incipiente tema de la electroquímica.
El nombre de galvanoplastia se debe a Luigi Galvani (Bolonia, Italia, 1737-1798) quien fue un médico, fisiólogo y físico italiano.
De forma genérica bajo el nombre “galvanoplastia” se agrupan diversos procesos en los que se emplea el principio físico de electrodeposición de diferentes formas. La aplicación original a gran escala de la galvanoplastia era reproducir por medios electroquímicos objetos con detalles muy finos y en muy diversos metales. El primer empleo práctico fueron las planchas de imprenta hacia 1839.
El electroformado es un método para reproducir piezas de metal mediante deposición eléctrica. El proceso más utilizado a partir de la década de 1970 es la electrodeposición, o enchapado electrolítico, de un metal sobre una superficie a fin de mejorar sus características. Inicialmente, se utilizó por cuestiones estéticas, pero posteriormente se usó con el objetivo de mejorar las propiedades mecánicas de los objetos tratados: su dureza, su resistencia, etc.
La electroquímica moderna fue desarrollada por el químico italiano Luigi V. Brugnatelli (nacido en Pavía en 1805). Brugnatelli utilizó el invento que cinco años antes había hecho su colega Alessandro Volta, la pila voltaica, para realizar la primera electrodeposición.
Moritz Hermann Jacobi, posteriormente, introdujo mejoras en el proceso, por lo que se lo designa como “inventor de la galvanoplastia” o electrotipia, en 1838. Jacobi fue un científico prusiano que estaba trabajando en San Petersburgo (Rusia).
Los procesos de galvanoplastia o electrodeposición se dividen en dos: electroformación de láminas para moldes y revestimientos de protección. En el primer caso, suelen utilizarse metales como el estaño y el cromo; mientras que en el segundo caso, se utiliza frecuentemente níquel, cobre y plata.
El electroformado es un método para reproducir piezas de metal mediante deposición eléctrica. El proceso más utilizado a partir de la década de 1970 es la electrodeposición, o enchapado electrolítico, de un metal sobre una superficie a fin de mejorar sus características. Inicialmente, se utilizó por cuestiones estéticas, pero posteriormente se usó con el objetivo de mejorar las propiedades mecánicas de los objetos tratados: su dureza, su resistencia, etc.
La electroquímica moderna fue desarrollada por el químico italiano Luigi V. Brugnatelli (nacido en Pavía en 1805). Brugnatelli utilizó el invento que cinco años antes había hecho su colega Alessandro Volta, la pila voltaica, para realizar la primera electrodeposición.
Moritz Hermann Jacobi, posteriormente, introdujo mejoras en el proceso, por lo que se lo designa como “inventor de la galvanoplastia” o electrotipia, en 1838. Jacobi fue un científico prusiano que estaba trabajando en San Petersburgo (Rusia).
Los procesos de galvanoplastia o electrodeposición se dividen en dos: electroformación de láminas para moldes y revestimientos de protección. En el primer caso, suelen utilizarse metales como el estaño y el cromo; mientras que en el segundo caso, se utiliza frecuentemente níquel, cobre y plata.
Objetivos
El objetivo principal de la galvanoplastia o electrodeposición es modificar las propiedades de una superficie metálica de modo que se pueda proteger a la superficie de la corrosión, aumentar su resistencia a golpes y ralladuras, así como elevar su resistencia a ciertas sustancias químicas. La galvanoplastia es muy importante, ya que permite modificar las propiedades del metal base sin tener que rehacer una pieza, solo utilizando un simple concepto de electroquímica.
Además de proteger a la superficie de la pieza metálica de la corrosión y de efectos erosivos del ambiente, la galvanoplastia permite elevar la durabilidad de los materiales, así como cambiar las características de la superficie de los metales para hacerlos más conductores o resistentes al fuego, etc. Asimismo, es una técnica bastante económica, ya que permite revestir metales con costos relativamente bajos, ahorrando en aleaciones metálicas, algo de gran importancia para la industria.
Además de proteger a la superficie de la pieza metálica de la corrosión y de efectos erosivos del ambiente, la galvanoplastia permite elevar la durabilidad de los materiales, así como cambiar las características de la superficie de los metales para hacerlos más conductores o resistentes al fuego, etc. Asimismo, es una técnica bastante económica, ya que permite revestir metales con costos relativamente bajos, ahorrando en aleaciones metálicas, algo de gran importancia para la industria.
El objetivo principal de la galvanoplastia o electrodeposición es modificar las propiedades de una superficie metálica
Aplicaciones
- Bronceado o latonado. Como su nombre lo indica, consiste en aplicar una o varias capas de bronce o latón sobre una superficie, generalmente, a fin de modificar su apariencia.
- Cobreado. Su objetivo principal es depositar una capa de cobre sobre una superficie. Usualmente, se utiliza para elevar la conductividad eléctrica.
- Estañado. Aplicar capas de estaño a un metal es particularmente útil para proteger de la corrosión piezas de hierro en función de ciertas utilidades.
- Plateado. Al igual que el cobreado, es comúnmente utilizado para añadir capas de plata que permitan elevar la conductividad eléctrica de una superficie.
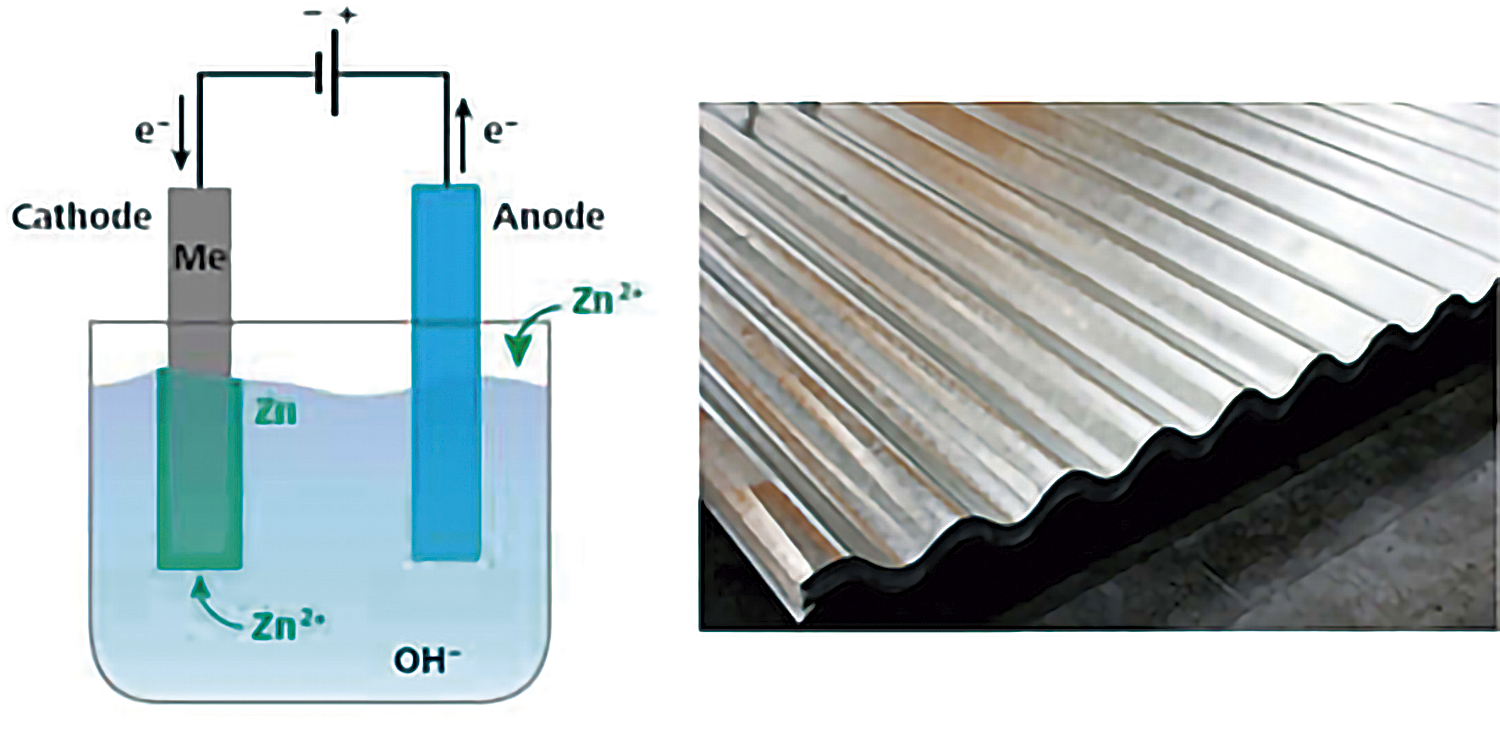
- Zincado. Aplicar electrolíticamente capas de zinc a una superficie permite protegerla de la corrosión, sobre todo, al hierro, así como mejorar la apariencia de la superficie.
- Plásticos metálicos. Consiste en aplicar una capa de plástico con propiedades conductoras sobre una superficie metálica y luego revestirlos de un metal, el cual se adhiere a la superficie del polímero como si fuese papel aluminio.
Proceso
Las etapas de un proceso industrial de galvanoplastia o electrodeposición son las siguientes: recepción de la materia prima, desengrase o limpieza química de las piezas que se van a tratar, lavado de desengrase, decapado o desoxidación de las piezas, lavado de decapado, preparación mecánica de las piezas, limpieza física de las piezas y electrólisis (cobreado, cromado, niquelado, zincado, etc).
El recubrimiento se realiza a través de un proceso de electrólisis. Se toma en cuenta la conservación de la masa, es decir, siempre debe haber material que se oxide y material que se reduzca. Se pueden realizar las reacciones de oxidación y reducción en recipientes separados unidos por conductores metálicos para que los electrones viajen libremente.
El recubrimiento se realiza a través de un proceso de electrólisis. Se toma en cuenta la conservación de la masa, es decir, siempre debe haber material que se oxide y material que se reduzca. Se pueden realizar las reacciones de oxidación y reducción en recipientes separados unidos por conductores metálicos para que los electrones viajen libremente.
A fin de lograr una galvanoplastia o electrodeposición efectiva, también se suelen utilizar materiales metálicos de recubrimiento como sulfatos, cloruros, entre otros.
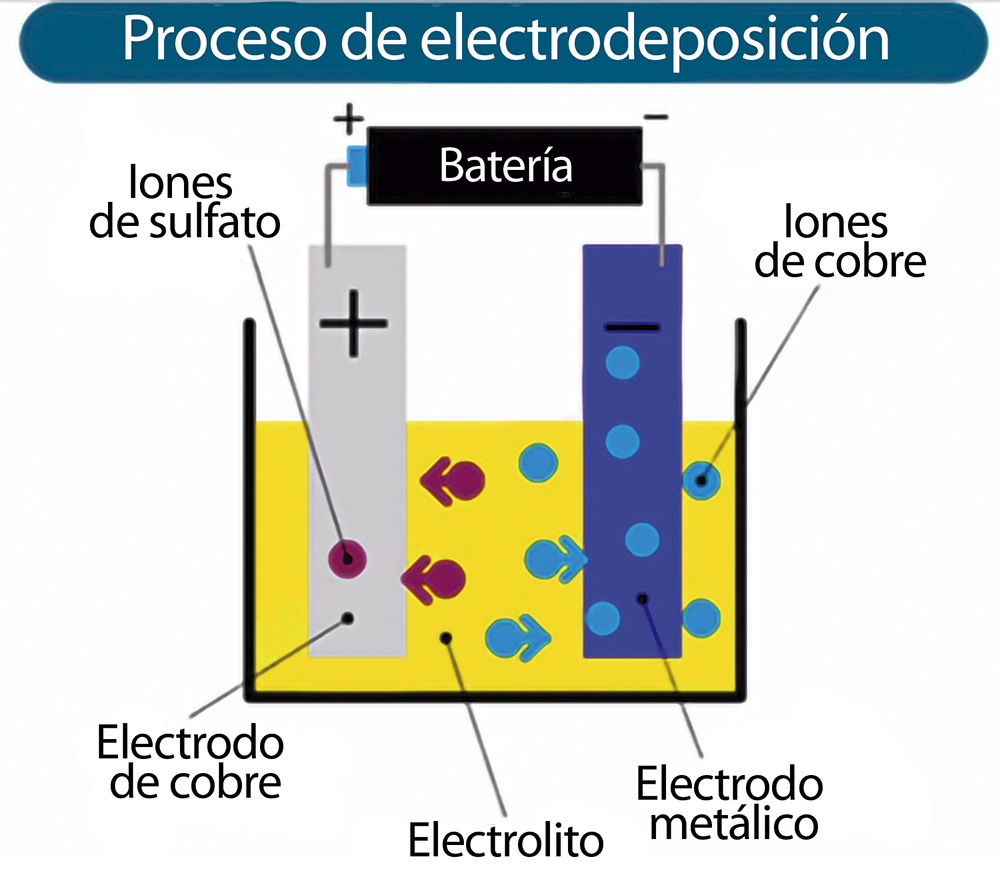
Cuando sucede la electrólisis, la solución conductora (electrolito) fomenta el viaje de los electrones del ánodo al cátodo mediante la aplicación de una corriente eléctrica. A fin de lograr una galvanoplastia o electrodeposición efectiva, también se suelen utilizar materiales metálicos de recubrimiento como sulfatos, cloruros, entre otros, hasta alcanzar las condiciones deseadas de la película de recubrimiento.
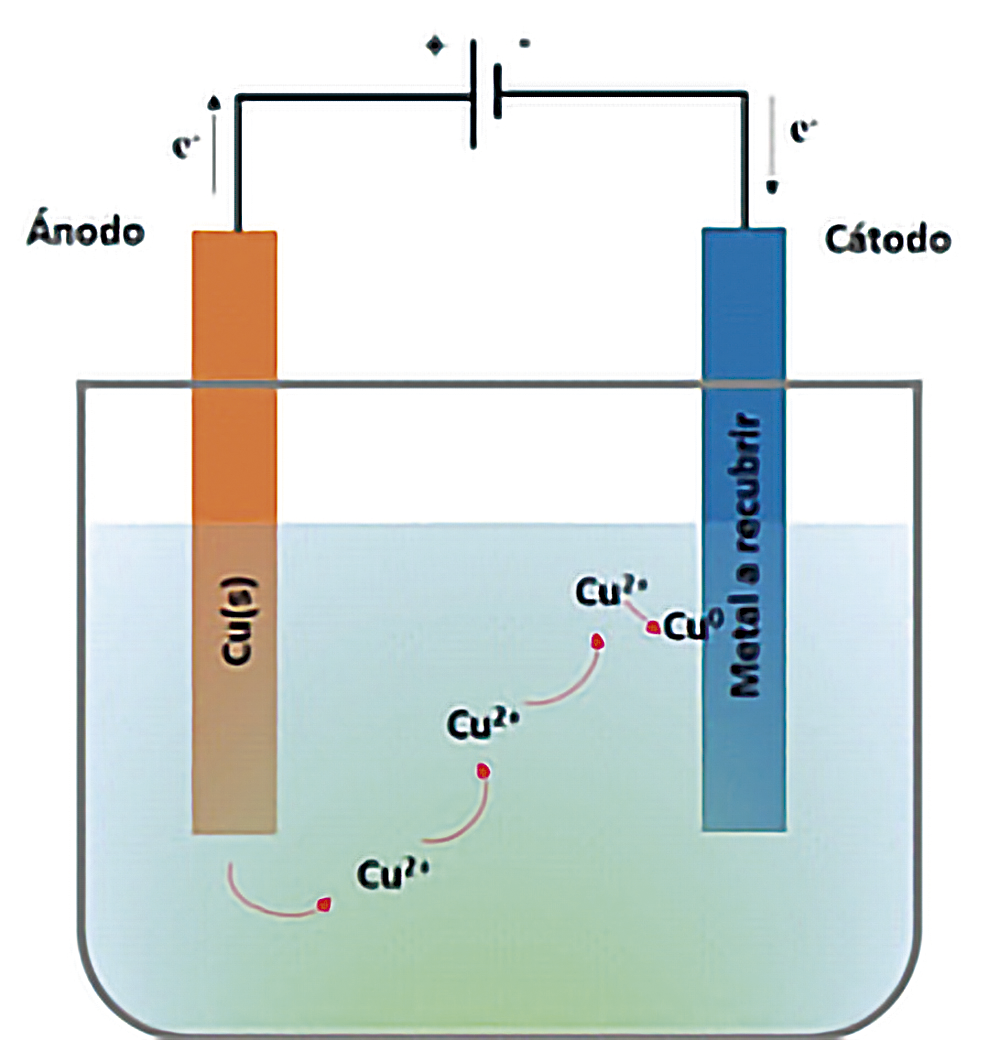
Por ejemplo, cobreado. Para realizarlo, se utiliza un ánodo de cobre y un cátodo, que será la pieza de metal que se desea recubrir. También se requiere de un circuito eléctrico externo donde el polo negativo se conecta al ánodo, el positivo al cátodo, y estos a una fuente de electricidad de corriente continua (ver figura 2).
Por ejemplo, cobreado. Para realizarlo, se utiliza un ánodo de cobre y un cátodo, que será la pieza de metal que se desea recubrir. También se requiere de un circuito eléctrico externo donde el polo negativo se conecta al ánodo, el positivo al cátodo, y estos a una fuente de electricidad de corriente continua (ver figura 2).
Una vez cerrado el circuito eléctrico, el cátodo comienza a cargarse negativamente y el ánodo, positivamente. Esto fomenta a los electrones de cobre a salir del ánodo y viajar a través de la solución salina hasta el cátodo, efectuando una reacción de reducción:
Cu2+ (ac) = 2e— → Cu(s)
A fin de mantener la neutralidad del electrolítico, se ejecuta simultáneamente gracias al uso de la fuente de electricidad, una reacción de oxidación en el ánodo:
Cu(s) → Cu2+ (ac) + 2e—
Así, los electrones que se liberan regresan eventualmente a la fuente eléctrica, y de allí se movilizan hacia el cátodo, de modo que la electrodeposición se siga realizando. Durante este proceso, el ánodo de cobre va perdiendo masa, mientras que el cátodo se reviste de una fina capa de cobre que le otorgará nuevas propiedades a su superficie.
Cu2+ (ac) = 2e— → Cu(s)
A fin de mantener la neutralidad del electrolítico, se ejecuta simultáneamente gracias al uso de la fuente de electricidad, una reacción de oxidación en el ánodo:
Cu(s) → Cu2+ (ac) + 2e—
Así, los electrones que se liberan regresan eventualmente a la fuente eléctrica, y de allí se movilizan hacia el cátodo, de modo que la electrodeposición se siga realizando. Durante este proceso, el ánodo de cobre va perdiendo masa, mientras que el cátodo se reviste de una fina capa de cobre que le otorgará nuevas propiedades a su superficie.
Bibliografia
[1] https://www.ingenieriaquimicareviews.com/2021/06/que-es-la-galvanoplasti...
[2] https://es.wikipedia.org
[3] García González, Carlos Alberto, Técnicas y métodos electroquímicos: galvanoplastia y potenciometría, Universidad Técnica de Machala, Ecuador.
[4] López, Karla, Galvanoplastia.
[1] https://www.ingenieriaquimicareviews.com/2021/06/que-es-la-galvanoplasti...
[2] https://es.wikipedia.org
[3] García González, Carlos Alberto, Técnicas y métodos electroquímicos: galvanoplastia y potenciometría, Universidad Técnica de Machala, Ecuador.
[4] López, Karla, Galvanoplastia.
Por Ricardo Berizzo
Autor:
Publicado en:
Número:
Mes:
Año: